科学与研发
糖脂代谢疾病
糖脂是一类多样化的生物活性分子,在各种正常和致病的细胞过程中发挥作用。代谢不同糖脂的酶的遗传缺陷可导致在不同细胞类型的溶酶体中糖脂异常积累。这种积累可能具有多种致病作用,并导致一系列称为溶酶体贮积病(LSD)的疾病。根据严重程度和所涉及的特定糖脂,这些LSD会影响各种身体器官,包括心脏,肾脏,肝脏,在某些情况下还可以影响中枢神经系统。
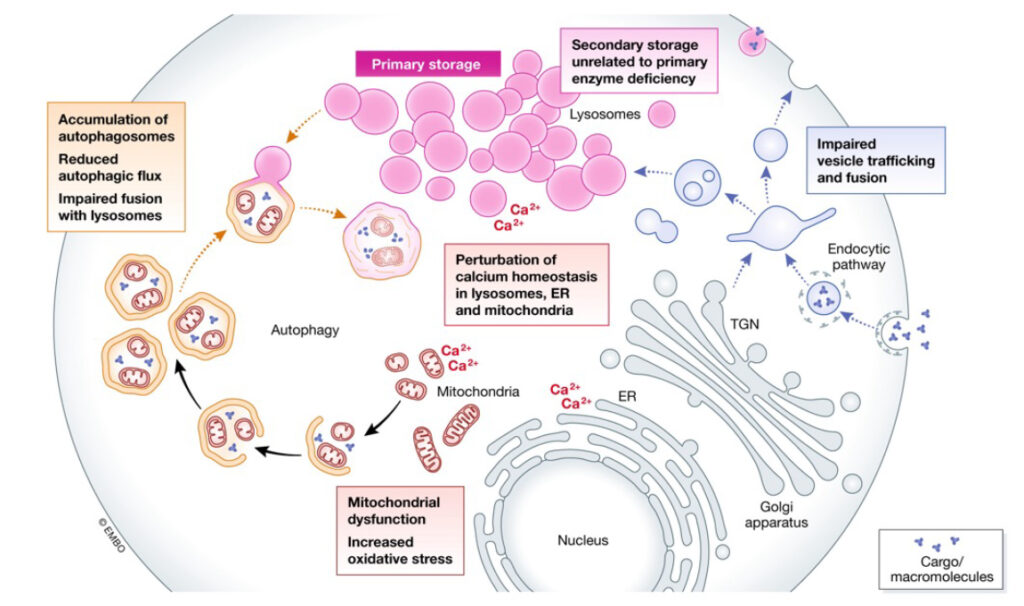 Parenti et al. EMBO MolMed. 2021
Parenti et al. EMBO MolMed. 2021
通过抑制合成这些糖脂的关键酶GCS,我们通过减少致病性糖脂的产生来解决疾病的根源。这种方法称为底物减少疗法(SRT)。AceLink正在开发大脑靶向和非大脑靶向的小分子疗法,以治疗不同的LSD。可以用SRT治疗的LSD包括法布雷病、戈谢病以及GM1和GM2神经节苷脂贮积症等。
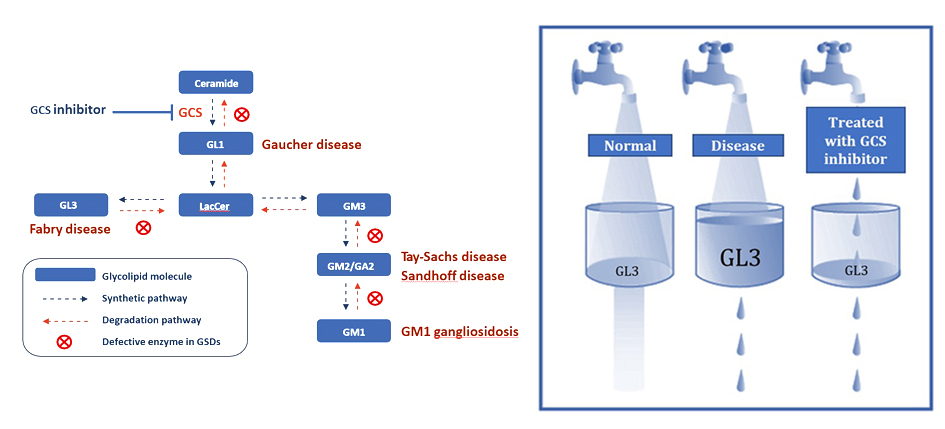
糖脂在慢性疾病中也会失调,它们会导致与疾病相关的炎症、细胞增殖、蛋白质错误折叠和纤维化。这些疾病包括多囊肾病、糖尿病肾病、脂肪肝、心脏病,甚至帕金森病。对于这些疾病,降低特定糖脂的细胞水平也可以起到治疗作用。
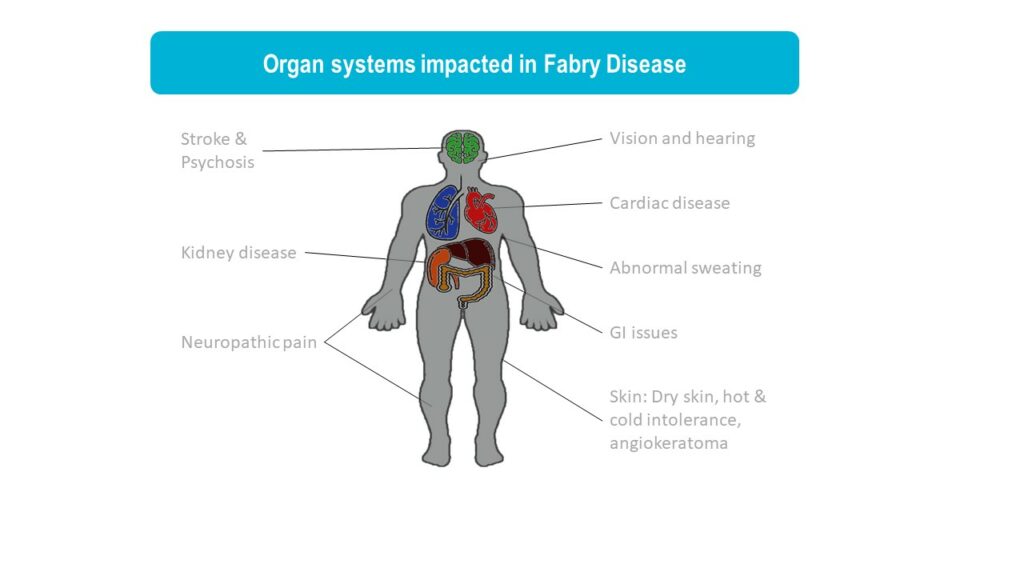
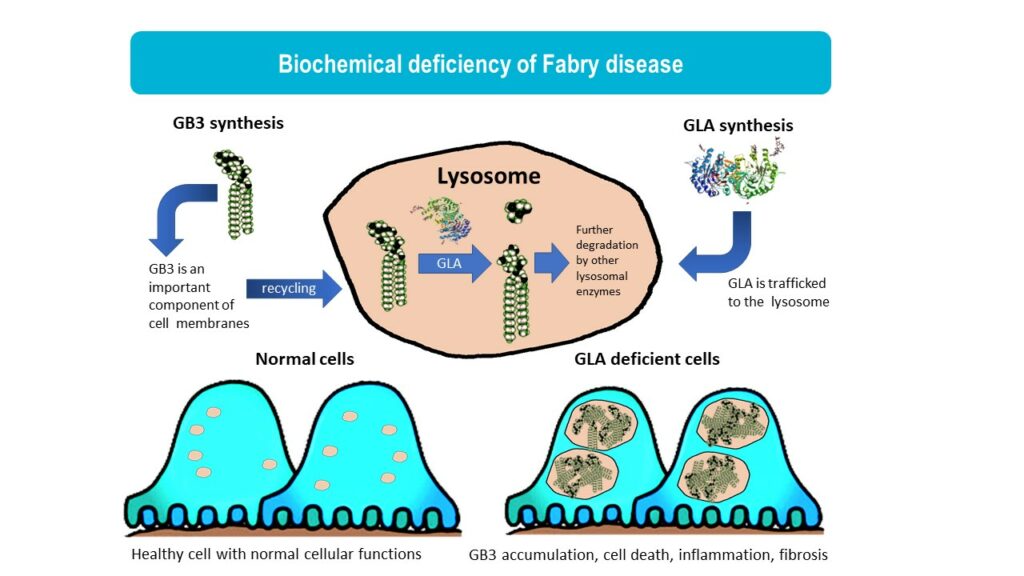
法布雷病是一种溶酶体贮积症,由GLA基因突变引起,导致α-半乳糖苷酶A(αGal)活性降低。在法布雷病患者中,αGal活性缺失会导致球形三酰神经酰胺(GL3)积累,导致从疼痛、胃肠道问题、眼睛和皮肤问题到肾衰竭、心脏病和中风等一系列症状。法布雷病是一种X连锁疾病,在男性中更常见,但女性也可能患上法布雷病,但通常程度较轻。传统观点认为每50,000名男性中有1名受到法布雷病的影响。然而,随着新生儿筛查、女性中对法布雷病认识的加强以及晚发形式法布雷病的鉴定,现在人们认识到大约每1,000至9,000人中就有1人患有法布雷病(Medline)。
酶替代疗法(ERT)是法布雷病的标准治疗方法。虽然ERT减少了许多法布雷症状的进展,但由于酶对某些细胞类型的渗透率低,其益处是不完全的。许多接受ERT治疗的患者仍然发展为进展性的肾脏和心脏病。ERT还有其他缺点,如成本高,终身静脉输注负担以及对ERT的过敏反应。ERT的局限性凸显了对安全有效的小分子口服疗法的需求,这些疗法可以更有效地穿透不同的细胞类型和组织。
AceLink正在开发一种GCS抑制剂AL01211来治疗法布雷病。
戈谢病是由GBA1基因突变引起的溶酶体贮积症(糖脂贮积症)。GBA1 突变导致溶酶体酶葡萄糖脑苷脂酶 (GCase)的活性降低。在戈谢病患者中,GCase活性缺乏导致葡萄糖神经酰胺(GL1)及其代谢产物lyso-GL1的在体内的积累。根据GCase缺乏的严重程度,戈谢病患者可出现II型和III型戈谢病所见的神经系统症状,也可出现较轻的非神经系统症状,如I型戈谢病。
已有上市的酶替代疗法(ERT)和小分子底物减少疗法(SRT)用于戈谢病。虽然ERT减少了许多戈谢病症状的进展但这些药物不能解决戈谢病的神经系统特征,因为它们不能穿过血脑屏障。
AceLink正在开发脑渗透性的口服小分子SRT药物(AL0804),将用于治疗戈谢病的CNS和非CNS症状。
GM1神经节苷脂贮积症是由GLB1基因突变引起的溶酶体贮积症。GLB1突变导致溶酶体中 β-半乳糖苷酶(βGal)活性降低。在 GM1 神经节苷脂贮积症患者中,βGal缺乏导致GM1 神经节苷脂(GM1)的积累。具有最严重βGal缺乏的GM1神经节苷脂贮积症患者会出现严重的早发性神经系统症状,而轻度βGal缺乏可导致晚发性神经系统症状。
GM2神经节苷脂贮积症是由HEXA或HEXB基因突变引起的一组溶酶体贮积症。Tay-Sachs 病是由HEXA基因突变引起的GM2神经节苷脂贮积症的一种形式,Sandhoff 病是由 HEXB 基因突变引起的。HEXA和HEXB一起编码β-氨基己糖苷酶的蛋白质亚基。HEXA或HEXB 突变导致溶酶体酶β-氨基己糖苷酶(βHex)活性降低。在GM2神经节苷脂贮积症患者中,βHex缺乏导致GM2神经节苷脂(GM2)的积累。具有最严重βHex缺乏的GM2神经节苷脂贮积症患者会出现严重的早发性神经系统症状,而较轻的βHex缺乏可导致晚发性神经系统症状。
AceLink正在开发可用于治疗GM1和GM2神经节苷脂贮积症的脑渗透性小分子SRT。
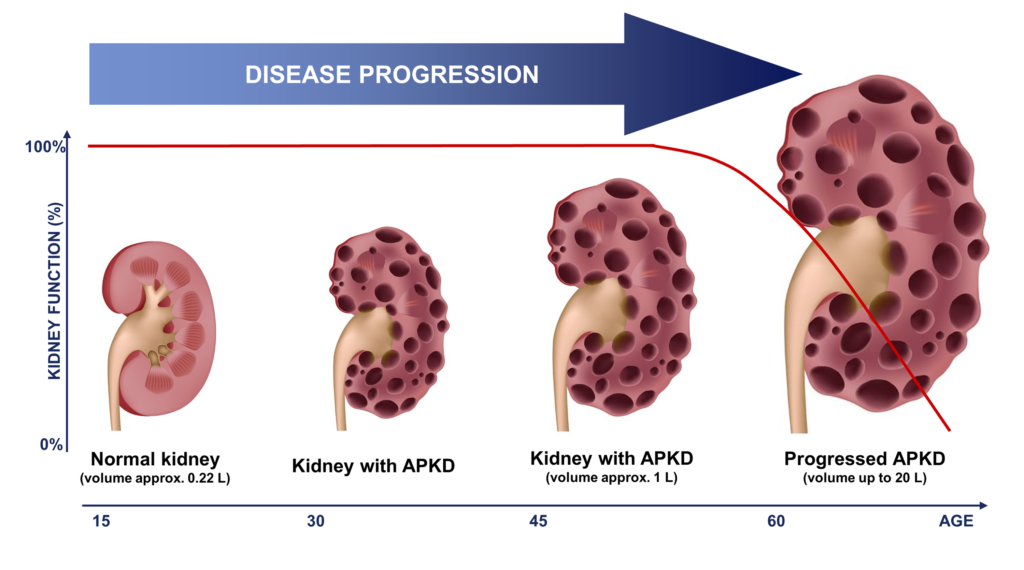
常染色体显性遗传性多囊肾病(ADPKD)是一种遗传性疾病,主要在肾脏内形成大量囊肿,导致肾脏扩大并最终失去功能。ADPKD是最常见的遗传性肾脏疾病,其特征是出现许多充满液体的囊肿、肾脏增大,并最终进展为慢性肾脏病(CKD)和终末期肾病(ESRD)。虽然一些严重形式的ADPKD会影响幼儿,但大多数PKD患者在成年早期或更晚时出现症状。进展为ESRD的可能性随着年龄的增长而增加,60岁以上的ADPKD患者中有50%需要透析或肾移植。大多数ADPKD病例是由两个基因PKD1和PKD2其中之一的突变引起的。这两个基因编码的蛋白质定位于肾上皮细胞的初级纤毛,在调节肾脏发育和功能、促进上皮分化、防止细胞增殖方面发挥重要作用。
鞘糖脂GL1和GM3在PKD患者和PKD动物模型的肾组织中升高。在多种不同的PKD动物模型中使用GCS抑制剂的研究表明,减少鞘糖脂的产生可以减缓囊肿生长并保护肾功能。
Natoli TA, Modur V, Ibraghimov-Beskrovnaya O. Glycosphingolipid metabolism and polycystic kidney disease. Cell Signal. 2020 May;69:109526. doi: 10.1016/j.cellsig.2020.109526. Epub 2020 Jan 10. PMID: 31911181.
Natoli TA, Smith LA, Rogers KA, Wang B, Komarnitsky S, Budman Y, Belenky A, Bukanov NO, Dackowski WR, Husson H, Russo RJ, Shayman JA, Ledbetter SR, Leonard JP, Ibraghimov-Beskrovnaya O. Inhibition of glucosylceramide accumulation results in effective blockade of polycystic kidney disease in mouse models. Nat Med. 2010 Jul;16(7):788-92. doi: 10.1038/nm.2171.
GBA突变相关性帕金森病可以说是帕金森病最常见的遗传形式。大量遗传研究表明,GBA1基因(导致戈谢病的基因)的单个突变可使患帕金森病的风险增加多达30倍。体外和体内的临床前研究表明,α-突触核蛋白蛋白可以与糖脂相互作用并导致聚集和毒性。在帕金森病小鼠模型中使用GCS抑制剂的研究支持,降低这些糖脂的产生可以减少突触核蛋白聚集,减缓神经行为表型的进展和神经退行性病变。
Vieira SRL, Schapira AHV. Glucocerebrosidase mutations and Parkinson disease. J Neural Transm (Vienna). 2022 Sep;129(9):1105-1117. doi: 10.1007/s00702-022-02531-3. Epub 2022 Aug 6.
Sardi SP, Viel C, Clarke J, Treleaven CM, Richards AM, Park H, Olszewski MA, Dodge JC, Marshall J, Makino E, Wang B, Sidman RL, Cheng SH, Shihabuddin LS. Glucosylceramide synthase inhibition alleviates aberrations in synucleinopathy models. Proc Natl Acad Sci U S A. 2017 Mar 7;114(10):2699-2704. doi: 10.1073/pnas.1616152114. Epub 2017 Feb 21.
糖尿病肾病(DN)是一种常见的肾损伤形式,随着I型和II型糖尿病等代谢疾病的进展而发生。如果糖尿病没有得到适当的治疗,那么肾小球(肾脏的过滤单位)可能会受到损害。这种损害可导致高血压,从而给肾脏带来更大的压力并导致更多的损害、慢性肾脏疾病(CKD)并最终进展为终末期肾病(ESRD)。
糖脂已被证实在代谢性疾病中发挥作用。糖脂水平升高可致胰岛素抵抗,使用 GCS抑制剂降低糖脂可以增加胰岛素敏感性并改善葡萄糖耐量。糖脂在糖尿病肾病患者的肾脏中升高,它们可能导致炎症、肥大和纤维化。因此,用GCS抑制剂治疗患者可以靶向糖尿病肾病中发生的代谢性疾病和由此产生的组织损伤。
